
Práctica 3: Diagrama de Clapeyron y curva de presión de vapor saturado
- 1 | Introducción y fundamento teórico
- 2 | Materiales
- 3 | Realización

- 4 | Resultados y discusión
Desarrollo de la práctica
El estudio del punto crítico requiere del uso de elevadas presiones. Se advierte a los estudiantes que deben seguir de forma minuciosa las instrucciones que se dan a continuación, sin superar los límites establecidos y dando cuenta al profesor de cualquier incidencia que tuviera lugar en el transcurso de la práctica.
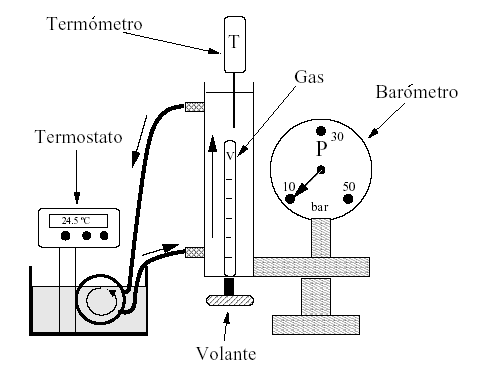
Figura 2: Esquema de montaje experimental utilizado para el estudio del diagrama de Clapeyron y curva de vaporpara el vapor saturado.
Para llevar a cabo esta práctica se requiere medir para cinco temperaturas diferentes la presión en el interior del tubo de pruebas conforme se varía el volumen del gas en su interior. Hay que tener en cuenta que se parte del volumen máximo (4ml) y se va disminuyendo, por lo que estamos reconstruyendo la isoterma desde la derecha hacia la izquierda en la figura (1b). La toma de medidas se realiza de la forma siguiente:
- Conectar la camisa de vidrio que rodea al tubo de pruebas al termostato de inmersión, y poner el agua en circulación. La primera medida se tomará a temperatura ambiente por lo que no se debe conectar la resistencia del termostato. Ver esquema del montaje en la figura2.
- Colocar el termómetro digital en el tapón que cubre el tubo de vidrio que contiene al tubo de pruebas de forma que esté en la vertical del tubo de pruebas y en contacto con el agua de recirculación.
- Una vez que la temperatura que marque el termómetro digital se haya estabilizado tomar esta como temperatura de partida.
- Registrar en la tabla 1 el valor que adquiere la presión al variar el volumen del gas, variando el volumen con el giro del volante de mano que se encuentra al pie del tubo de pruebas (Ver figura 2). Las medidas se tomarán a intervalos regulares del volumen (por ejemplo 0.25 ml), o como el estudiante crea más conveniente, pero siempre obteniendo al menos quince puntos para cada isoterma.
- IMPORTANTE: Téngase en cuenta que se están tomando medidas en la isoterma de derecha a izquierda, por lo que una vez que se ha condensado todo el vapor y estamos en la zona de líquido la presión variará muy bruscamente. No llevar nunca a la zona de peligro la medida de presión y, en todo caso, no llevar el volumen a valores menoresde 0.4ml.
- A medida que disminuya el volumen llegará un momento en el que comience la condensación del gas. El momento en el que se inicia la condensación resulta fácilmente perceptible si se observan las paredes del tubo de pruebas, por las que comienza a resbalar el líquido, acumulándose sobre el menisco de mercurio. Registrar en la tabla ese momento con un asterisco en el valor de la presión en el que haya tenido lugar.

Descargar el video de opalescencia crítica
- Una vez que se haya completado la toma de datos experimentales para la temperatura ambiente a la que se realice la práctica (RECUERDE: No llevar nunca el volumen a valores menores de 0.4ml) se tomarán de la misma forma que se ha descrito valores de la presión para los mismos volúmenes con cuatro temperaturas más. Para ello se pondrá en marcha el termostato de inmersión y se esperará a que se estabilice en el valor deseado la temperatura del termómetro junto al tubo de pruebas 1 y se retorna la columna de mercurio al valor original del volumen (4 ml). La temperatura máxima que se alcanzará es de aproximadamente 45ºC, muy cercana a la temperaturacrítica de Tc = 45.5ºC, las temperaturas intermedias que se alcancen deben cubrir de forma adecuada el rango entre la temperatura ambiente y esta última temperatura. Para fijar la temperatura pulse en el termostato el botón SET y simultáneamente las flechas arriba o abajo hasta alcanzar el valor deseado.
- Tras la toma de datos experimentales se representarán el diagrama de Clapeyron y la curva de presión del vapor saturado para el hexafluoruro de azufre.
Es importante que una vez se termine la toma de datos se desconecte el termostato de inmersión y se baje la presión al mínimo en el tubo de pruebas.
Capacidades y conocimientos que se deben adquirir
- Ser capaz de obtener los datos experimentales para construir el diagrama de Clapeyron para el hexafluoruro de azufre.
- Ser capaz de construir la curva
presión de saturación frente a la temperatura para el hexafluoruro de azufre. - Ser capaz de ver la equivalencia entre los resultados obtenidos y el caso del vapor de agua.
1 Se recomienda para poder terminar la práctica en el tiempo establecido aprovechar el tiempo de espera para comenzar la representación del diagrama de Clapeyron con los datos previamente obtenidos.









